コンテンツ
SN反応
置換反応のこと
SN1反応
一分子で進む反応、二段階で進みます。(1系)
SN1の進みやすさは置換基が抜けた後の化合物の安定性によって決まります。
SN2反応
二分子で進む反応、一段階で進みます。(1系)
E反応
脱離反応、二重結合が生成します。
E1反応
一分子で進む反応、二段階で反応します。(1系)
E2反応
二分子で進む反応、一段階で進行します。(2系)
脱離反応では脱離基の位置による生成物の選択性がある場合があります。
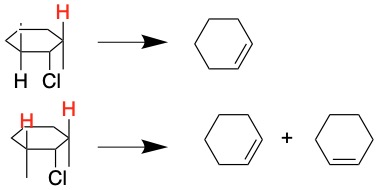
E2反応で脱離する場合、反対側で脱離する水素の位置は決まっています。図のClが脱離する場合、赤字の水素が脱離します。上の化合物では脱離できる水素が1つしかないので、生成物は一種類になります。
見分け方
1系か2系か
試薬に使用される塩基の強さで、1系か2系を見分けることができます。
強塩基→2系
弱塩基→1系
強塩基は求核性が強いため1段階で進むことができます。弱塩基は求核性が弱いため、基質を一度カチオンにしてから出ないと反応を進めることができません。
第一級アルキルでは、弱塩基であってもSN1反応は進みません。第一級カルボカチオンはかなり不安定だからです。
脱離か置換か
1系の場合
SN1とE1の競合(SN1の方が進みやすい)
2系の場合
| 第一級 | 第二級 | 第3級 |
| 置換 | 置換または脱離 | 脱離 |
かさだかい(めっちゃ官能基がついてる)ほど、置換しようとして求核剤が近づいても官能基がブロックするため置換ができません。また求核剤のかさだかさも影響してきます。
例外
第一級カルボカチオンであってもアリルカチオンやベンジルカチオンは例外的にSN1反応が進みます。
例題
1
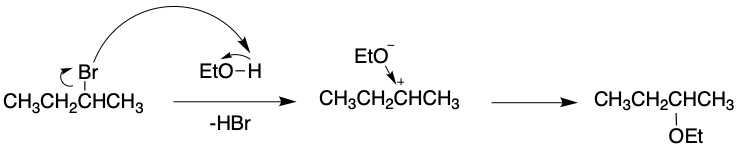
SN1反応で進みます。試薬が弱塩基なので1系であることがわかり、1系では置換と脱離が競合するので、とりあえず置換で回答すればOKです。(a-1-1)
2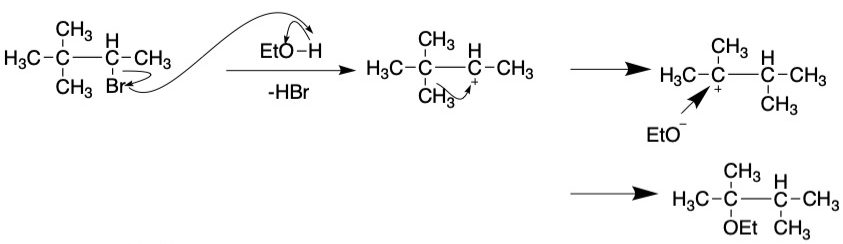
SN1反応+アルキル基の転移反応で進みます。弱塩基のため1系であることがわかり、2段階目と3段階目のカチオンのついた炭素を見ます。三段階目の炭素のほうが超共役によって安定化することがわかります。従ってアルキル転移を行います。(a-1-2)
3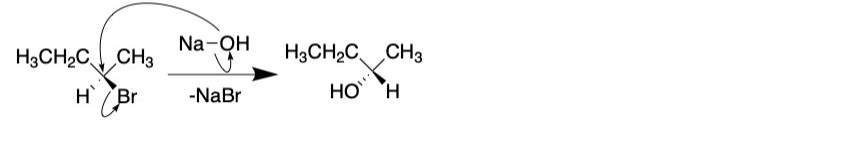
SN2で進みます。強塩基のため2系で進みます。2系の場合、置換基は脱離基と反対側から近づくため立体の構造が決定します。(a-1-3)
4
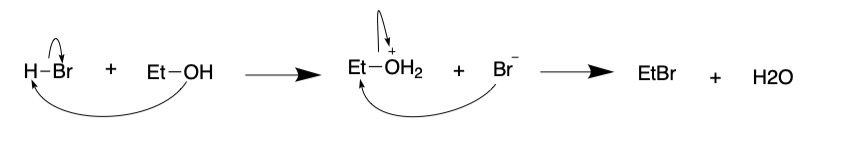
SN2反応で進みます。第1級のため2系の置換反応が進みます。(a-2-1)
5
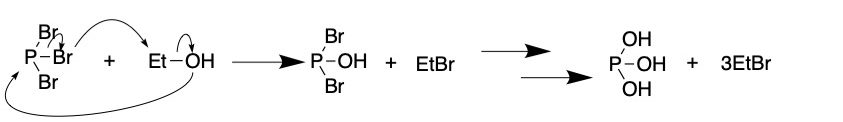
SN2反応で進みます。三臭化リンは、構造が三角錐のようになっているため立体障害が小さくなります。従ってこの場合は、SN2反応で進みます。また、PBr3は最後まで反応を進めて書く必要があるためこのような反応式になります。(a-2-2)
6
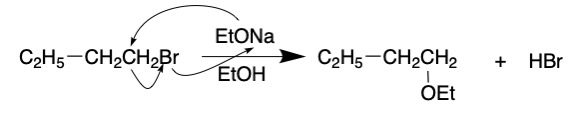
SN2反応で進みます。EtONaは強塩基です。EtOとNaのイオンになったときにEtOは弱酸のため、Hが結合します。Naは、OHと結合しないので結果として強塩基になります。強塩基なので2系の反応が進みます。第一級で立体障害もないのでSN反応になります。(a-3-1)
7
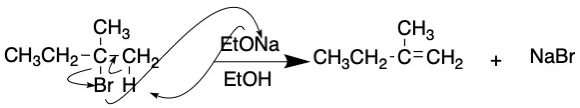
E2反応で進みます。強塩基なので2系が進みます。第3級のため脱離反応が進みます。(a-3-2)
8
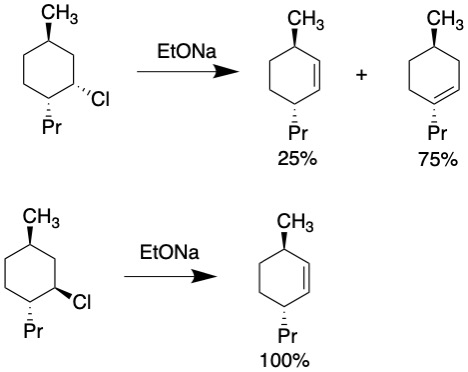
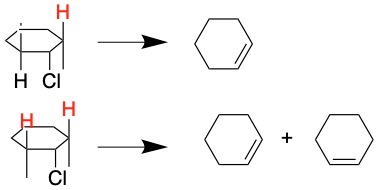
上の化合物では、E2反応によって脱離できる水素は2つあります。そのため2つの生成物が得られます。(a-5)